جدول المحتويات
مقدمة: التخطيط للتجارب السريرية Trial Planning
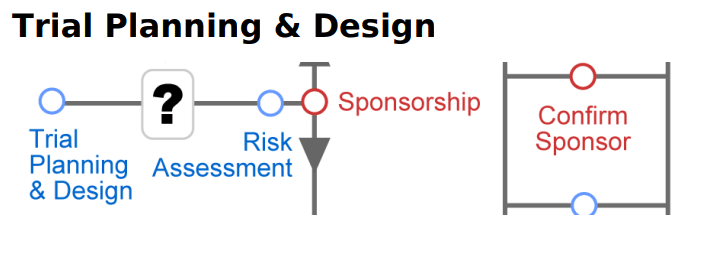
خريطة المسارات Routemap
Routemap
The Clinical Trials Toolkit is an interactive colour-coded routemap* to help navigate through the legal and good practice arrangements surrounding setting up and managing a Clinical Trial of an Investigational Medicinal Product (CTIMP). The routemap distinguishes between legal and good practice requirements, and indicates which aspects of these are relevant to wider clinical research in general. It includes an overview of trial practices, along with more detailed information available at ‘stations’ along the route.
*Mobile users will be able to access the stations from the list shown
Download a copy of the Clinical Trials Toolkit routemap (pdf, 221.33 KB) (.PDF).
خريطة المسارات
مجموعة أدوات التجارب السريرية هي خريطة مسارات تفاعلية مُرمّزة بالألوان* تُساعدك على التنقل عبر الترتيبات القانونية وقواعد الممارسات الجيدة المُتعلقة بإعداد وإدارة تجربة سريرية لمنتج طبي تجريبي (CTIMP). تُميّز خريطة المسارات بين المتطلبات القانونية وقواعد الممارسات الجيدة، وتُشير إلى جوانبها ذات الصلة بالبحوث السريرية الأوسع نطاقًا بشكل عام. تتضمن الخريطة لمحة عامة عن ممارسات التجارب، بالإضافة إلى معلومات أكثر تفصيلًا مُتاحة في “المحطات” على طول المسار.
*سيتمكن مستخدمو الهواتف المحمولة من الوصول إلى المحطات من القائمة المُوضحة.
مرحلة تخطيط وتصميم التجربة Trial planning and design
تُعد مرحلة تخطيط التجربة وتصميمها المحطة الأولى في هذه الخريطة، وتسبق تأكيد ما إذا كانت التجربة تندرج ضمن نطاق لوائح التجارب السريرية، ومحطة تقييم المخاطر. يُعد تخطيط التجربة وتصميمها ممارسة جيدة، وهي ذات صلة بجميع التجارب. وتندرج هذه المحطة ضمن مجموعة محطات “مرحلة تخطيط التجربة”.
تتمة
يُعدّ تصميم التجربة المتين أمرًا أساسيًا لضمان نجاحها. ينبغي دراسة تصميم التجربة قبل وضع البروتوكول. سيساعد ذلك على ضمان تحديد جميع المتطلبات العملية اللازمة مبكرًا، مما يُمكّن من طلب التمويل الكافي.
تُسهّل خطة الدراسة الموثقة جيدًا عملية إعداد طلبات التمويل، وموافقات لجنة الأخلاقيات، وموافقات البحث والتطوير/أذونات هيئة الخدمات الصحية الوطنية، وأي موافقات تنظيمية ضرورية.
غالبًا ما تشترك التجارب الناجحة في خصائص متشابهة. وهي:
بسيطة من الناحية النظرية ومُصممة خصيصًا لمجموعة المرضى
تُعالج المسائل ذات الأهمية السريرية عند وجود شكوك حقيقية
تجنّب معايير الإدخال المُعقّدة/المُقيّدة بشكل غير ضروري لضمان إمكانية التعميم، عند الاقتضاء
تجنّب متطلبات البيانات المُعقّدة بشكل غير ضروري (الناتجة عن تبرير دقيق لكل نقطة بيانات سيتم جمعها)
ضمان اختيار ذراع التحكم الأنسب (عند الاقتضاء)
ضمان إخفاء التخصيص بشكل دقيق (عند الإمكان)
ضمان التعمية الدقيقة للتدخل أو تقييمات النتائج المُعمّاة بشكل مناسب (عند الاقتضاء).
من المهم التعاون مع إحصائي يمكنه المساعدة في:
تصميم تجربتك
اختيار النتيجة المناسبة
تبرير حجم العينة
تقديم المشورة بشأن منهجية التوزيع العشوائي المناسبة
وضع خطة للتحليل الإحصائي
معالجة البيانات المجمعة وهيكلتها
إعداد التقارير المؤقتة وتقديمها إلى لجان مراقبة البيانات (DMCs)، إن وجدت.
تُعدّ مشاركة المرضى والجمهور (PPI) أمرًا بالغ الأهمية لضمان أهمية السؤال المقترح وارتباطه بالأشخاص الذين يؤثر عليهم مباشرةً، ولضمان أن تكون التجربة عملية وقابلة للتنفيذ. وتتوافر الآن قاعدة أدلة متنامية تدعم الأثر الإيجابي الذي يمكن أن تُحدثه مشاركة المرضى والجمهور على استقطاب المشاركين في التجارب السريرية واستبقائهم فيها. ويشترط العديد من الممولين إثبات المشاركة الحقيقية كشرط للتمويل.
الملف الاصلي هنا
(Trial planning and design (Trial Planning Phase
Trial planning and design is the first station on this routemap and precedes confirming whether a trial falls within the scope of the Clinical Trial Regulations, and the Risk Assessment station. Trial Planning & Design is good practice and is relevant to all trials. This station is part of the ‘trial planning phase’ group of stations.
A robust trial design is essential to ensure a successful outcome. The trial design should be considered before developing the protocol. This will help ensure that all necessary practical requirements are identified early so that adequate funds are requested.
A well-documented study plan will facilitate the process of developing funding applications, ethics committee and R&D approvals / NHS permissions, and any necessary regulatory approvals.
Successful trials often share similar characteristics. They are:
Conceptually simple and tailored to the patient group
Address questions of clinical relevance where genuine uncertainties exist
Avoid unnecessarily complex/restrictive entry criteria to ensure generalisability, where appropriate
Avoid unnecessarily complex data requirements (resulting from a careful justification of each data point to be collected)
Ensure the most appropriate choice of control arm (where appropriate)
Ensure robust allocation concealment (where possible)
Ensure robust blinding of intervention or appropriately blinded outcome assessments (where appropriate).
It is important to collaborate with a statistician who can help with:
Designing your trial
Choosing an appropriate outcome
Providing justification of the sample size
Advising on appropriate randomisation methodology
Drawing up a statistical analysis plan
Handling and structuring collected data
Preparing and presenting interim reports to Data Monitoring Committees (DMCs), if applicable.
Patient and public involvement (PPI) is important to ensure that the question proposed is important and relevant to the people it directly affects and that the trial is practical and feasible. There is now a growing evidence base to support the positive impact that PPI can have on participation recruitment and retention in clinical trials. Many funders will require evidence of genuine involvement as a condition of funding.
The Health Research Authority have launched Best Practice Principles for Public Involvement that describes four key principles.
The National Context:
When initiating a trial, researchers should familiarise themselves with the framework in place for conducting trials. In particular:
1) The role of the National Institute of Health Research (NIHR), the process and criteria for inclusion of research on the NIHR Research Delivery Network Portfolio and the importance of public and patient involvement when conducting research.
The NIHR Research Support Service (RSS) supports researchers in England to develop and design high quality research proposals for submission to NIHR and other national, peer-reviewed funding competitions for applied health or social care research (see Funding Proposal station).
2) The role of the UK Clinical Research Collaboration (UKCRC), which provides information on the infrastructure for research in the UK. Their web pages include information on Research Delivery Network and Clinical Trial Units (CTUs), including the process for identifying CTUs that may have expertise in coordinating multi-site research in different disease areas or with different trial designs (see UKCRC Registered CTU Networks).
3) The critical path for undertaking a clinical trial can be complex. The positioning of the stations on the route maps within this Toolkit also indicate which activities can be conducted in parallel and which activities should be completed before moving on the to the next stage.
For those new to managing trials, the NIHR Trial Managers Network (TMN) is a source of practical support and guidance on the trial management process.
4) The MRC-NIHR Trials Methodology Research Partnership (TMRP) promotes and encourages collaborative methodological research relevant to trials, with the aim of accelerating implementation of the most effective and appropriate methods. It supports workshops, conference and training in trials methodology, in addition to acting as a resource to highlight events and courses across the UK.
The MRC HTMR Network also collates outputs from various projects and initiatives under their “Guidance Pack” for trials.
The Network and individual Hubs also offer assistance to colleagues based in Clinical Trials Units and the Research Support Service when they receive enquiries, through the Methodology Advisory Service for Trials.
Further reading
MRC Ethics Series: Good Research Practice: Information published by the MRC giving guidelines on conducting research with human participants and their tissues and data.
Planning a Randomised Controlled Trial: Points to Consider : A paper summarising some of the trial activities that would need to be considered.
The NHS Research & Development Forum: The NHS R&D Forum is a network for those involved in managing and supporting R&D in health and social care. Information on key activities and developments is regularly updated.
Trainees Clinical Trial Guidance to support NIHR trainees interested in getting involved in clinical trials.
DIRUM is an open-access Database of Instruments for Resource Use Measurement.
Recommendations for the design of MAMS (multi-arm multi-stage) trials.
Avery et al. (.PDF) (2017) outlines the key issues to consider in the optimal development and review of operational progression criteria for RCTs with an internal pilot phase. Ten top tips (.PDF) for developing and using progression criteria for internal pilot studies are proposed.
Gamble et al. (2017) recommend a minimum set of items that should be addressed and included in Statistical Analysis Plans for clinical trials.
Lancet Series on Research Waste:
Avoidable waste in the production and reporting of research evidence by I Chalmers & P Glasziou.
Increasing value and reducing waste in research design, conduct, and analysis by J Ioannidis et al.
Medicinal Research Council (MRC) Resources:
The MRC hosts The Experimental Medicine Toolkit and resources supporting research using health data and human tissue samples.
Further resources on Patient and Public Involvement
Healthtalk.org showcases a range of different experiences in healthcare including participation and involvement in health research.
The NIHR Centre for Engagement and Dissemination leads NIHR’s work to make health and care research representative, relevant and ready for use. The centre brings together its activities in patient and public involvement (PPI), engagement and participation with its strengths in research dissemination. The NIHR also provides a range of resources for PPI and for the evaluation of PPI.
Two papers from the EPIC study (Evidence base for Patient and Public Involvement in Clinical trials) provide evidence to inform trial teams in planning for PPI in trials and optimising the impact of PPI.
The People in Research website can be used to help find public contributors to involve in research, or for public contributors to find opportunities to get involved in research.
مرحلة خضوع التجربة للوائح التجارب السريرية Within the scope of the Clinical Trial Regulations
تقع عملية التأكد من خضوع التجربة لنطاق لوائح التجارب السريرية within the scope of the Clinical Trial بين محطة تخطيط وتصميم التجربة ومحطة تقييم المخاطر. هذه عملية قياسية، وهذه المحطة جزء من مجموعة محطات “مرحلة تخطيط التجربة”.
تتمة
وكالة تنظيم الأدوية والرعاية الصحية (MHRA) هي الجهة المختصة بتنظيم لوائح الأدوية للاستخدام البشري (التجارب السريرية) في المملكة المتحدة. قبل بدء التجربة، من المهم التأكد من خضوعها لنطاق لوائح الأدوية للاستخدام البشري (التجارب السريرية) لعام 2004، والتي يُشار إليها، مع تعديلاتها، باسم لوائح التجارب السريرية ضمن هذه المجموعة. وقد أعدت MHRA خوارزمية (PDF) (.PDF) لمساعدة الباحثين على تحديد ما إذا كانت تجربتهم خاضعة للوائح الأدوية للاستخدام البشري (التجارب السريرية).
يجب على الباحثين الذين يخططون لتجارب CTIMP أن يكونوا على دراية بصفحات التجارب السريرية التابعة لـ MHRA لضمان مراعاة جميع المتطلبات القانونية.
مرحلة ما بعد خروج بريطانيا من الاتحاد الأوروبي
لم يعد التوجيه الأوروبي (2001/20/EC) (ملف PDF، 152 كيلوبايت) ساريًا في المملكة المتحدة. تُعدّل لوائح الأدوية للاستخدام البشري (التجارب السريرية) (التعديل) (خروج الاتحاد الأوروبي) لوائح الأدوية للاستخدام البشري (التجارب السريرية) لعام 2004 لتمكين وكالة تنظيم الأدوية ومنتجات الرعاية الصحية (MHRA) من العمل كجهة تنظيمية خارج الاتحاد الأوروبي.
أصدرت وكالة تنظيم الأدوية ومنتجات الرعاية الصحية (MHRA) إرشادات جديدة للتجارب السريرية على المؤسسات اتباعها.
الملف الاصلي هنا
The trial falls within the scope of the Clinical Trial Regulations
Confirming whether a trial falls within the scope of the Clinical Trial Regulations sits between the Trial Planning and Design station and the Risk Assessment station. This is a standard process and this station is part of the ‘trial planning phase’ group of stations.
The Medicines and Healthcare Regulatory Agency (MHRA) is the competent authority that regulates CTIMPs in the UK. Before a trial can begin, it is important to confirm whether it falls within the scope of the Medicines for Human Use (Clinical Trials) Regulations 2004, which together with its amendments, are referred to as the Clinical Trial Regulations within this Toolkit. The MHRA has produced an algorithm (PDF) (.PDF) to help researchers determine whether their trial is a CTIMP.
Researchers planning a CTIMP should be familiar with the MHRA Clinical Trials Pages to help ensure all legal requirements are considered.
Brexit Transition
The European Directive (2001/20/EC) (PDF, 152 KB) no longer applies in the UK. The Medicines for Human Use (Clinical Trials) (Amendment) (EU Exit) Regulations amend the Medicines for Human Use (Clinical Trials) Regulations 2004 to enable the MHRA to operate as a regulator outside the EU.
The MHRA has published new guidance for clinical trials for organisations to follow.
مرحلة تخطيط التجربة:محطة تقييم المخاطر The Risk Assessment station
المرحلة الثانية وهي محطة تقييم المخاطر تلي محطة تخطيط وتصميم التجربة، وتؤكد ما إذا كانت التجربة تندرج ضمن نطاق لوائح التجارب السريرية. يُعد تقييم المخاطر ممارسة جيدة ومناسبة لجميع التجارب.
تتمة:
قد لا تتمكن بعض المنظمات المضيفة من رعاية التجارب السريرية للمنتجات الطبية التجريبية (CTIMPs)، أو قد ترعى تجارب ذات مستوى مخاطرمعينة فقط. لذلك، من الضروري إشراكها في مرحلة مبكرة، وإجراء تقييم للمخاطر منذ البداية. يمكن تحديد العملية بحيث يُجرى تقييم المخاطر بناءً على مقترح البحث، ثم يُحسّن بعد صياغة البروتوكول.
التكيف مع المخاطر
طبّقت هيئة تنظيم الأدوية ومنتجات الرعاية الصحية (MHRA) خطةً لتحديد المخاطر المرتبطة بكل تجربة سريرية من خلال اعتماد استراتيجية مزدوجة:
تحديد مخاطر التجارب السريرية التجريبية (IMP) باستخدام تصنيف بسيط للمخاطر (الأنواع أ، ب، ج) بناءً على حالة التسويق والرعاية الطبية القياسية.
تحديد المخاطر المرتبطة بإجراء التجارب من خلال دراسة تصميم التجربة وسكانها وإجراءاتها لتحديد مواطن الضعف المحددة وتحديد كيفية التخفيف من أي مخاطر.
نُشرت “المناهج المُكيّفة مع المخاطر لإدارة التجارب السريرية للمنتجات الطبية التجريبية” (PDF) كجزء من منتدى MHRA للممارسات السريرية الجيدة لمساعدة الرعاة على القيام بهذه العملية.
يوفر موقع MHRA الإلكتروني مزيدًا من المعلومات من خلال قسم “الأسئلة الشائعة” في منتدى MHRA GCP المتعلق بتكييف المخاطر.
مزيد من القراءة ووثائق مسار العمل:
محطة الرعاية.
محطة إدارة التجارب ومراقبتها. وثيقة مشروع اليقظة الدوائية المشترك (pdf، ٣٤٤.٠٥ كيلوبايت).
محطة مستلزمات التجارب.
الملف الاصلي
The Risk Assessment station
The Risk Assessment station follows the Trial Planning and Design station, and confirming whether a trial falls within the scope of the Clinical Trial Regulations. Risk Assessment is good practice and is relevant to all trials. This station is part of the ‘trial planning phase’ group of stations.
Some host organisations may not be in a position to undertake the role of sponsor for Clinical Trials of Investigational Medicinal Products (CTIMPs) or may only sponsor trials of a certain risk level. It is essential therefore that they are involved at an early stage and that a risk assessment is undertaken at the very start. The process could be defined such that the risk assessment is undertaken on the research proposal and then further refined once the protocol has been drafted.
Risk Adaptation
The MHRA have implemented a scheme for defining the risks associated with each clinical trial by adopting a dual strategy:
Defining the risks of the IMP using a simple IMP risk categorisation (Type A,B and C) based on marketing status and standard medical care
Defining the risks associated with trial conduct by examining the trial design, population and procedures to identify specific areas of vulnerability and to determine how any risks can be mitigated.
The Risk-adapted Approaches to the Management of Clinical Trials of Investigational Medicinal Products (.PDF) has been published as part of the MHRA Good Clinical Practice Forum to help sponsors undertake this process.
The MHRA web site gives further information with a ‘Frequently Asked Questions’ thread on the MHRA GCP forum relating to risk adaptation.
Further reading & Workstream Documents:
Trials Management & Monitoring station.
Joint Project Pharmacovigilance Document (pdf, 344.05 KB).
Previous SectionWithin the scope of the Clinical Trial Regulations?Next SectionSponsorship
محطة الرعاية The Sponsorship station
تلي محطة الرعاية محطة تقييم المخاطر، وتسبق عملية موازية يتم خلالها وضع البروتوكول وإجراء مشاورات البحث والتطوير. الرعاية متطلب قانوني ينطبق على جميع التجارب. هذه المحطة جزء من مجموعة محطات “مرحلة تخطيط التجربة”.
تتمة
الرعاية مطلوبة للدراسات التي تُجرى بموجب إطار سياسة المملكة المتحدة لأبحاث الرعاية الصحية والاجتماعية، بما في ذلك التجارب التي تندرج ضمن نطاق لوائح التجارب السريرية. قد يستغرق تأمين راعٍ/رعاة بعض الوقت*، لذا يجب مراعاة تحديد الراعي في مرحلة مبكرة من عملية التخطيط.
*ملاحظة: يمكن لأكثر من جهة رعاية تجربة سريرية واحدة. يُشار إلى ذلك بالرعاية المشتركة.
فيما يتعلق بالتجارب السريرية للمنتجات الطبية التجريبية (CTIMPs)، يُعرّف مصطلح الراعي في لوائح التجارب السريرية بأنه: الشخص الذي يتحمل مسؤولية بدء تلك التجربة وإدارتها وتمويلها (أو ترتيب تمويلها). يجب أيضًا ذكر اسم الشخص (أو الأشخاص) المسؤول (أو الأشخاص) عن وظائف الراعي في تصريح التجارب السريرية (CTA).
يتحمل الراعي مسؤوليات قانونية محددة بموجب لوائح التجارب السريرية. قبل بدء أي تجربة، يجب على الراعي تحديد جميع الواجبات والوظائف المتعلقة بالتجربة وتأسيسها وتوزيعها. تقدم وثيقة مبادئ رعاية منتدى البحث والتطوير التابع لهيئة الخدمات الصحية الوطنية (NHS) ملخصًا شاملاً للمتطلبات، بما في ذلك نماذج الرعاية المختلفة وإرشادات حول توزيع المسؤوليات أو الواجبات أو الوظائف.
خروج بريطانيا من الاتحاد الأوروبي (Brexit)
اعتبارًا من 1 يناير 2021، يجب على الرعاة البريطانيين الذين يُجرون برامج إدارة التجارب السريرية (CTIMPs) في مواقع في المنطقة الاقتصادية الأوروبية (EEA) تعيين ممثل قانوني في دولة مدرجة في قائمة الدول المعتمدة (وهي حاليًا جميع دول الاتحاد الأوروبي/المنطقة الاقتصادية الأوروبية). يمكن الاطلاع على مزيد من الإرشادات حول متطلبات الممثل القانوني في وثيقة مبادئ الرعاية. بالإضافة إلى ذلك، أصدرت هيئة تنظيم الأدوية ومنتجات الرعاية الصحية (MHRA) إرشادات حول متطلبات التعديلات الجوهرية المتعلقة بتغيير الراعي أو الممثل القانوني للتجربة السريرية.
قراءات إضافية:
التأمين والتعويض في حالة الإصابة في التجارب السريرية للمرحلة الأولى: (PDF). إرشادات وضعتها جمعية صناعة الأدوية البريطانية، وجمعية الصناعات البيولوجية، وجمعية أبحاث العقود السريرية، بالتشاور مع وزارة الصحة والهيئة الوطنية لأخلاقيات البحث.
صفحات منتدى البحث والتطوير التابع لهيئة الخدمات الصحية الوطنية: موارد وتدريب ومجتمع ممارسات للمنظمات الراعية غير التجارية.
بريكست:
إرشادات بشأن التعديلات الجوهرية على التجارب السريرية.
الملف الاصلي
The Sponsorship station
The Sponsorship station follows the Risk Assessment station and precedes a parallel process in which the Protocol is developed and R&D Consultation takes place. Sponsorship is a legal requirement which is relevant to all trials. This station is part of the ‘trial planning phase’ group of stations.
Sponsorship is required for studies under the UK Policy Framework for Health and Social Care Research including trials that that fall within the scope of the Clinical Trial Regulations. It may take some time to secure a sponsor(s)*, so identification of the sponsor must be considered early in the planning process.
*Note: More than one entity can sponsor a clinical trial. This is referred to as joint or co-sponsorship.
For Clinical Trials of Investigational Medicinal Products (CTIMPs), the term sponsor is defined in the Clinical Trial Regulations as: the person who takes responsibility for the initiation, management, and financing (or arranging the financing) of that trial. The person(s) responsible for the sponsor’s functions must also be named on the Clinical Trial Authorisation (CTA).
The sponsor has specific legal responsibilities under the Clinical Trials Regulations. Before initiating a trial, the sponsor should define, establish and allocate all trial-related duties and functions. The NHS R&D Forum Sponsorship Principles document provides a comprehensive summary of requirements, including various models of sponsorship and guidance on the allocation of responsibilities, duties or functions.
Brexit
From 1st January 2021, UK sponsors conducting CTIMPs with sites in the European Economic Area (EEA), must establish a legal representative in a country on the approved country list (currently all countries in the EU/EEA). Further guidance on the requirements for a legal representative can be found in the Sponsorship Principles document. In addition, the MHRA has produced guidance on the requirements for substantial amendments relating to changing the sponsor or legal representative of a clinical trial.
Further reading
- Insurance and compensation in the event of injury in Phase I clinical trials: (.PDF) Guidance developed by the Association for the British Pharmaceutical Industry, the Bio Industry Association and the Clinical Contract Research Association, in consultation with the Department of Health and the National Research Ethics Service.
- NHS R&D Forum webpages: Resources, training and a community of practice for non-commercial sponsor organisations.
Brexit:
محطة تطوير البروتوكول The Protocol Development station
تلي محطة تطوير البروتوكول محطة الرعاية، وتتم بالتوازي مع مشاورات البحث والتطوير، ومقترح التمويل، ومراجعة الأقران. تسبق مرحلة تطوير البروتوكول محطة إدارة التجربة ورصدها. يُعد تطوير البروتوكول متطلبًا قانونيًا ينطبق على جميع التجارب. وتندرج هذه المحطة ضمن مجموعة محطات “مرحلة تخطيط التجربة”.
تتمة
يُعرّف البروتوكول في الجزء 1(2) من لوائح الأدوية للاستخدام البشري (التجارب السريرية) لعام 2004 بأنه: “وثيقة تصف أهداف التجربة السريرية، وتصميمها، ومنهجيتها، والاعتبارات الإحصائية، وتنظيمها”.
يوفر البروتوكول معلومات حول خلفية التجربة ومبرراتها، ويحدد خطة الدراسة. يجب تصميم الخطة بعناية لضمان صحة وسلامة المشاركين، بالإضافة إلى الإجابة على أسئلة البحث.
يجب أن يصف البروتوكول جميع جوانب التجربة، وأن يُصاغ بوضوح ودقة، وأن يضمن تجنب التجربة لأي تعقيد غير ضروري (ICH GCP E6 R2). يجب أن تتضمن البروتوكولات تعريفًا لنهاية التجربة (انظر محطة إعلان نهاية التجربة) ومعلومات عن الرعاية بعد التجربة.
يجب أن تكون البروتوكولات (والعديد من الوثائق الأخرى المُعدّة كجزء من التجربة) وثائق مُراقبة؛ وأن تُرقّم الإصدارات وتُؤرّخ وفقًا لقواعد رسمية.
تُساعد مشاركة المرضى والجمهور (PPI) في صياغة الجوانب الأساسية للبروتوكول لضمان مراعاته لاحتياجات المشاركين. يُمكن العثور على معلومات وموارد مفيدة حول PPI في محطة تخطيط وتصميم التجربة.
قد تُقدّم خدمة دعم أبحاث المعهد الوطني للبحوث الصحية (RSS) الدعم فيما يتعلق بجوانب تطوير البروتوكول، مثل تصميم التجربة، واختيار مقاييس النتائج المناسبة، والمدخلات الإحصائية للباحثين المقيمين في إنجلترا.
لدعم الباحثين في تطوير بروتوكولات عالية الجودة، أصدرت هيئة أبحاث الصحة إرشاداتٍ خاصة بالبروتوكولات ونموذجًا قابلًا للتنزيل لمساعدة المؤسسات والأفراد على تحسين اتساق وجودة برامجهم البحثية التدخلية (CTIMPs).
يتوافق النموذج مع المتطلبات التنظيمية وإرشادات SPIRIT (بنود البروتوكول القياسية: توصيات للتجارب التدخلية). على الرغم من أن النموذج ليس إلزاميًا، إلا أنه يتضمن جميع العناصر التي ترغب هيئات المراجعة في أخذها في الاعتبار، لذا فإن البروتوكولات التي تراعي الإرشادات والنموذج أقل عرضة لإثارة الاستفسارات التي قد تسبب تأخيرًا.
بالنسبة للبحوث غير التابعة لبرنامج CTIMP، يُنصح بتضمين أكبر قدر ممكن من المعلومات الواردة في مواضيع/أقسام ICH GCP E6 وقائمة التحقق SPIRIT، حسب الاقتضاء.
يعتمد كلٌ من SPIRIT وبرنامج NIHR HTA قاعدة بيانات COMET التي تحتوي على معلومات حول دراسات مجموعة النتائج الأساسية المنشورة والجارية، والتي يتم تحديثها بانتظام.
DIRUM هي قاعدة بيانات مفتوحة المصدر لاستبيانات استخدام الموارد، مخصصة لخبراء اقتصاديات الصحة المشاركين في التقييمات الاقتصادية القائمة على التجارب. يوفر DIRUM أيضًا مستودعًا للأوراق المنهجية المتعلقة باستخدام الموارد وقياس التكلفة.
يمكن الاطلاع على معلومات حول مراجعة البروتوكول والموافقة عليه في محطة البروتوكول النهائي.
للمزيد من القراءة:
محطة تسجيل التجارب
محطة البروتوكول النهائي
محطة التعديلات الجوهرية
SPIRIT (بنود البروتوكول القياسية: توصيات للتجارب التدخلية) هي مبادرة دولية تهدف إلى تحسين جودة بروتوكولات التجارب السريرية.
توصيات لتصميم تجارب MAMS (متعددة الأذرع ومتعددة المراحل)
يوصي Gamble وآخرون (2017) بمجموعة دنيا من البنود التي ينبغي تناولها وإدراجها في خطط التحليل الإحصائي للتجارب السريرية.
الملف الاصلي
The Protocol Development station
The Protocol Development station follows the Sponsorship station and takes place in a parallel process with R&D Consultation, the Funding Proposal, and Peer Review. Protocol Development precedes the Trial Management & Monitoring station. Protocol Development is a legal requirement which is relevant to all trials. This station is part of the ‘trial planning phase’ group of stations.
A protocol is defined in Part 1(2) of The Medicines for Human Use (Clinical Trials) Regulations 2004 as: “A document that describes the objectives, design, methodology, statistical considerations, and organisation of a clinical trial”
The protocol provides information on the background and rationale for a trial and outlines the study plan. The plan must be carefully designed to safeguard the health and safety of the participants, as well as answer the research question(s).
The protocol should describe all aspects of the trial but should also be written to be clear and concise and should also ensure that the trial avoids ‘unnecessary complexity’ (ICH GCP E6 R2). Protocols should include a definition of the ‘end of the trial’ (see End of Trial Declaration station) and information on post-trial care.
Protocols (and many other documents produced as part of a trial) should be controlled documents; version numbered and dated using a formalised convention.
Involvement of patients and the public (PPI) helps to shape fundamental aspects of the protocol to ensure it takes into account the needs of participants. Useful information and resources about PPI can be found in the Trial Planning & Design station.
The NIHR Research Support Service (RSS) may provide support relating to aspects of protocol development such as trial design, choosing appropriate outcome measures and statistical input for researchers based in England.
To support researchers to develop high quality protocols, the Health Research Authority have produced protocol guidance and a template download to assist organisations and individuals to improve the consistency and quality of their CTIMPs. The template is in line with regulatory requirements and the SPIRIT guidelines (Standard Protocol Items: Recommendations for Interventional Trials). Although the template is not mandatory, it contains all the elements that review bodies wish to consider, so protocols which have regard for the guidance and template are less likely to raise queries that can cause delays.
For non-CTIMP research, it is good practice for the protocol to include as much of the information in the topics/sections of ICH GCP E6 and the SPIRIT checklist, as relevant.
Both SPIRIT and the NIHR HTA Programme endorse the COMET database which contains information on published and ongoing core outcome set studies, and is regularly updated.
DIRUM is an open-access database of resource-use questionnaires for use by health economists involved in trial-based economic evaluations. DIRUM also provides a repository of methodological papers related to resource use and cost measurement.
Information on protocol review and signoff can be found in the Final Protocol station.
Further reading
Gamble et al. (2017) recommend a minimum set of items that should be addressed and included in Statistical Analysis Plans for clinical trials.
SPIRIT (Standard Protocol Items: Recommendations for Interventional Trials) is an international initiative that aims to improve the quality of clinical trial protocols
Recommendations for the design of MAMS (multi-arm multi-stage) trials
مرحلة تخطيط التجربة Trial Management & Monitoring
تلي إدارة التجربة ومراقبتها محطة تطوير البروتوكول وتسبق محطة توثيق التجربة. تُعد إدارة التجربة ومراقبتها متطلبًا قانونيًا ينطبق على جميع التجارب. تُعدّ هذه المحطة جزءًا من مجموعة محطات “مرحلة تخطيط التجربة”.
يُساعد التخطيط المُناسب قبل التجربة، والإشراف والمراقبة الكافيان خلالها، على ضمان الحفاظ على سلامة المشاركين طوال فترة التجربة، وتقديم تقارير دقيقة عن النتائج عند انتهائها.
تتمة
يتحمل الراعي مسؤولية ضمان وضع أنظمة قوية لإدارة التجارب. تُعد مراقبة التجربة أحد الأنشطة الرئيسية المُتخذة كجزء من إدارة التجربة. تتبنى وكالة تنظيم الأدوية ومنتجات الرعاية الصحية (MHRA) نهجًا مُكيفًا مع المخاطر لإدارة التجارب،
ويمكن الاطلاع على النصائح الخاصة بمراقبة التجارب في الملحق 2 من “النهج المُكيفة مع المخاطر لإدارة التجارب السريرية للمنتجات الطبية التجريبية” (pdf).
تُعالج إدارة التجارب المُكيّفة مع المخاطر السؤال التالي:
ما هي العمليات والبيانات الأساسية لهذه التجربة، وكيف يُمكن التخفيف من أي مخاطر أو نقاط ضعف مُحددة في هذه المجالات على أفضل وجه؟
ينبغي دراسة هذا السؤال مُبكرًا في مرحلة تصميم البروتوكول، بحيث يُمكن وضع إجراءات لإدارة جوانب التجربة الحيوية للجودة بشكل استباقي. وقد أصدرت مبادرة تحويل التجارب السريرية الأمريكية (CTTI) مجموعة أدوات تتضمن مبادئ الجودة من خلال التصميم (PDF) تُوفر إطارًا عمليًا لهذه العملية.
في حال إسناد أنشطة إدارة التجارب إلى جهات خارجية، يجب على الجهة الراعية تطبيق إجراءات لضمان الإشراف المناسب على جميع الوظائف المُفوّضة. ويمكن تحقيق ذلك من خلال:
تقييم مدى تأهيل الأفراد أو المؤسسات المُفوّضة لمهام إدارة التجارب وكفاءتهم لأداء هذه الوظائف.
التأكد من أن جميع الأطراف على دراية بأدوارهم ومسؤولياتهم (على سبيل المثال، من خلال تحديدها بوضوح في العقود والاتفاقيات).
الحفاظ على خطوط اتصال لضمان الوفاء بالتزامات جميع الأطراف (على سبيل المثال، من خلال استلام تقارير التقدم).
ينبغي توفير توثيقات لوصف جميع العمليات الرئيسية. يضمن ذلك أن يكون لدى القائمين على المهام خطة واضحة حول ماهية أنشطة المحاكمة وتوقيتها وكيفية تنفيذها، كما يُمكّن المدققين/المفتشين من إعادة بناء جميع أنشطة إدارة المحاكمة تاريخيًا.
فيما يلي معلومات وإرشادات إضافية حول إدارة التجارب:
يقدم ملخص وثيقة مسار عمل أنظمة إدارة التجارب لمحة عامة عن الأنشطة المرتبطة بإدارة التجارب، بالإضافة إلى متطلبات الإشراف عليها وتوثيقها.
يقدم وثيقة مسار عمل إجراءات الرصد معلومات إضافية حول أنواع الرصد التي يمكن للراعي تنفيذها (على سبيل المثال، الرصد في الموقع أو الرصد الإحصائي المركزي) وتوثيق جميع جوانب عملية الرصد. كما تقدم وثائق مسار عمل المشروع المشترك التالية أمثلة إضافية على التكيف مع المخاطر:
سيناريوهات التجارب في الرصد، والتي توضح نهج الرصد المطبق على خمس تجارب مختلفة تمامًا.
يوفر برنامج NIHR Learn تدريبًا لدعم الموظفين المشاركين في التجارب السريرية، بما في ذلك تدريب ممارسات الممارسة السريرية الجيدة (GCP) وتدريبًا للموظفين في أقسام الخدمات مثل الصيدليات والمختبرات.
يوضح دليل ممارسات الممارسة السريرية الجيدة (GCP) الصادر عن وكالة تنظيم الأدوية ومنتجات الرعاية الصحية (MHRA) توقعات إدارة التجارب ورصدها، ويقدم وصفًا مفصلاً لجميع العمليات الرئيسية والعديد من أمثلة التكيف مع المخاطر.
تُعد شبكة مديري التجارب (TMN) مصدرًا للدعم العملي والإرشاد حول عملية إدارة التجارب، وقد نشرت إرشادات شاملة بعنوان: “دليل الإدارة الفعالة للتجارب”.
يستضيف برنامج البحوث الطبية التابع للمعهد الوطني للبحوث الصحية (MRC-NIHR TMRP) سلسلة من الندوات الإلكترونية حول إدارة التجارب، بما في ذلك “مراقبة التجارب بكفاءة: دور المراقبة الإحصائية المركزية”.
توصي إرشادات إعداد التقارير الخاصة بالمعايير الموحدة لإعداد التقارير عن التجارب (CONSORT) بالاحتفاظ بسجل دقيق للمرضى الذين يُنظر في مشاركتهم في التجارب العشوائية المحكومة.
يوفر إطار عمل SEAR (الفحص، التأهيل، الاتصال، العشوائية) (PDF) طريقة منهجية لتسجيل تدفق المشاركين المحتملين خلال عملية التوظيف لدعم ممارسات توظيف أفضل في التجارب السريرية.
وُضعت إرشادات حول تعظيم تأثير البحث النوعي في دراسات الجدوى للتجارب العشوائية المحكومة لمساعدة الباحثين على النظر في النطاق الكامل للمساهمات التي يمكن أن يقدمها البحث النوعي فيما يتعلق بتجاربهم الخاصة.
يُحدد استخدام الأساليب النوعية لإثراء استبيانات دلفي في تطوير مجموعة النتائج الأساسية (PDF) بعض القضايا التي يجب على مطوري COS مراعاتها.
تطوير واستخدام معايير التقدم للدراسات التجريبية الداخلية: أفيري وآخرون. (2017) (PDF) يُحدد القضايا الرئيسية التي يجب مراعاتها في التطوير الأمثل ومراجعة معايير التقدم التشغيلي للتجارب السريرية العشوائية ذات المرحلة التجريبية الداخلية.
شبكة وحدات العلاج الكيميائي المسجلة في المملكة المتحدة – رصد التجارب السريرية: دليل، يُقدم معلومات حول نظرية الرصد، ونصائح سلوكية، وأمثلة واقعية قد تُساعد في شرح ودعم مناهج الرصد الممكنة وتطبيقاتها.
قراءات إضافية:
نشرت مجموعة عمل مفتشي الممارسات السريرية الجيدة (GCP) عددًا من الوثائق المتعلقة بإجراءات التجارب:
ورقة تأمل للمختبرات التي تُجري تحليلًا أو تقييمًا لعينات التجارب السريرية (ملف PDF، 135 كيلوبايت) (ملف PDF).
ورقة تأمل حول توقعات بيانات المصدر الإلكترونية والبيانات المنقولة إلى أدوات جمع البيانات الإلكترونية في التجارب السريرية (ملف PDF، 127 كيلوبايت) (ملف PDF).
تشترط العديد من الجهات الممولة والمجلات العلمية إتاحة بيانات المشاركين الأفراد من التجارب السريرية عند الطلب المعقول. يصف تيودور سميث وآخرون تطوير إرشادات مراكز أبحاث منهجية التجارب (HTMR) التابعة لمجلس البحوث الطبية (MRC) حول مبادئ الممارسات الجيدة لمشاركة بيانات المشاركين الأفراد من التجارب الممولة من القطاع العام.
يمكن الاطلاع على إرشادات الباحثين ومنسقي الدراسات حول قانون حماية البيانات العام على موقع هيئة تنظيم الموارد البشرية الإلكتروني.
خين وآخرون. سلامة البيانات في التجارب السريرية العالمية: مناقشات من ورشة عمل الممارسات السريرية الجيدة المشتركة بين إدارة الغذاء والدواء الأمريكية وهيئة تنظيم الأدوية ومنتجات الرعاية الصحية في المملكة المتحدة. علم الأدوية والعلاج السريري، المجلد 108، العدد 5.
انظر النص الاجنبي للارتباطات بالملفات المطلوبة
الملف الاصلي
Trial Management & Monitoring
follows the Protocol Development station and precedes the Trial Documentation station. Trial Management & Monitoring is a legal requirement which is relevant to all trials. This station is part of the ‘trial planning phase’ group of stations.
Appropriate planning before the trial and adequate oversight and monitoring during the trial will help ensure that trial subject safety is maintained throughout the trial and that there is accurate reporting of results at its conclusion.
The sponsor is responsible for ensuring that robust trial management systems are put in place. The monitoring of a trial is one of the key activities undertaken as part of the trial’s management.
The MHRA accepts a risk-adapted approach to trial management and the advice specific to trial monitoring can be found in Appendix 2 of The Risk-adapted Approaches to the Management of Clinical Trials of Investigational Medicinal Products (pdf) (.PDF).
Risk-adapted trial management addresses the question:
What are the critical processes and critical data for this trial and how best can any risks and/or vulnerabilities identified in these areas be mitigated?
This question should be considered early in the protocol design stage so that processes to proactively manage those aspects of the trial that are critical to quality can be put in place.
The US Clinical Trials Transformation Initiative (CTTI) have produced a Toolkit including Quality by Design principles (.PDF) that provides a useful framework for this process.
Where trial management activities are contracted out to third parties, the sponsor must implement procedures to ensure appropriate oversight of all delegated functions. This can be achieved by:
Assessing that individuals or organisations delegated trial management functions are appropriately qualified and competent to perform those functions.
Ensuring all parties are aware of their roles and responsibilities (for example by clearly defining them in contracts and agreements).
Maintaining lines of communication to ensure the obligations of all parties are being met (for example by receiving progress reports).
Documentation should be in place to describe all key processes. This ensures that those performing tasks have a clear plan of what, when and how trial activities are undertaken and also enables auditors/inspectors to historically reconstruct all trial management activities.
The following provide further information and guidance on trial management:
The Summary of Trial Management Systems Workstream Document gives an overview of the activities associated with trial management as well as the requirement for oversight and documentation of those activities.
The Monitoring Procedures Workstream Document gives further information on the types of monitoring a sponsor may implement (for example on-site monitoring or central statistical monitoring) and the documentation of all aspects of the monitoring process.
Further examples of risk adaptation are also provided in the following Joint Project Workstream Documents:
Trial Scenarios in Monitoring which illustrates the approach to monitoring applied to five very different trials
NIHR Learn provides training to support staff involved in clinical trials, including GCP training and training for staff in service departments such as pharmacy and laboratories.
The MHRA GCP Guide outlines the expectations for trial management and monitoring and provides a detailed description of all key processes and many examples of risk adaptation.
The Trial Managers Network (TMN) is a source of practical support and guidance on the trial management process and has published comprehensive guidance: A Guide to Efficient Trial Management.
The MRC-NIHR TMRP host a series of webinars on trial conduct including Monitoring trials efficiently: The role of central statistical monitoring.
Consolidated Standards of Reporting Trials (CONSORT) reporting guidelines recommend that an accurate record of patients considered for RCT participation is maintained.
The SEAR (Screened, Eligible, Approached, Randomised) framework (.PDF) provides a systematic way to record the flow of potential participants through the recruitment process to support better recruitment practices in clinical trials.
Guidance on maximising the impact of qualitative research in feasibility studies for RCTs was developed to help researchers consider the full range of contributions that qualitative research can make in relation to their particular trial.
The use of qualitative methods to inform Delphi surveys in core outcome set development (.PDF) identifies some issues for COS developers to consider.
Developing and using progression criteria for internal pilot studies: Avery et al. (2017) (.PDF) outlines the key issues to consider in the optimal development and review of operational progression criteria for RCTs with an internal pilot phase.
The UKCRC Registered CTU Network – Monitoring of clinical trials: a handbook, provides information on the theory of monitoring, tips on conduct and real life examples that may help to explain and support possible monitoring approaches and their application.
Further reading
The GCP Inspectors Working Group have published a number of documents relating to trial processes:
Several funders and journals require that Individual Participant Data from clinical trials are made available on reasonable request.
Tudur Smith et al describe the development of the MRC Hubs for Trials Methodology Research (HTMR) guidance on Good Practice Principles for Sharing Individual Participant Data from Publicly Funded Trials.
Guidance for researchers and study coordinators on the General Data Protection Act can be found on the HRA website.
Previous SectionProtocol DevelopmentNext SectionTrial Documentation



اترك تعليقاً